 Генная терапия снова подтвердила свой высокий потенциал, предотвратив поражение сетчатки. Ученые и врачи благодаря пересадке генов смогли излечить врожденное заболевание, грозящее полной потерей зрения в первые месяцы жизни.
Генная терапия снова подтвердила свой высокий потенциал, предотвратив поражение сетчатки. Ученые и врачи благодаря пересадке генов смогли излечить врожденное заболевание, грозящее полной потерей зрения в первые месяцы жизни.
В журнале Human Gene Therapy исследователи из Гарвардской медицинской школы представили описание серии экспериментальных операций на животных. Мышам, у которых развивался амавроз Лебера, пересадили в клетки сетчатки человеческий ген RPGRIP1, после чего процесс стремительной деградации светочувствительных клеток был остановлен. Как утверждают коллеги исследователей, специалисты медицинской школы при университете Массачусетса, разработанный метод обещает оказаться эффективным и безопасным способом предотвратить развитие слепоты и у людей.
Светлое будущее медицины
Генная терапия по праву считается фундаментом медицины будущего. Вместо того чтобы давать лекарства, вживлять протезы или пересаживать органы, врачи смогут целенаправленно исправлять дефекты ДНК в клетках. Если, к примеру, в кодирующем ключевой для зрения фермент гене содержится мутация, терапия пересадит в ДНК правильный вариант этого гена- и вернет зрение. Аналогично можно будет использовать знания о том, какие именно генетические ошибки вызывают рак, приводят к повышенному риску инфаркта и провоцируют иные заболевания, от редких наследственных патологий до таких распространенных, как сахарный диабет.
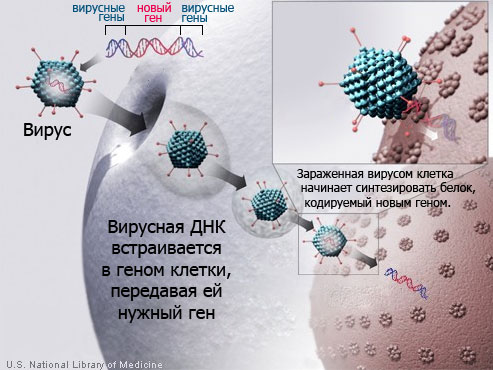
Так работает вирусная терапия - вирусы переделаны для того, чтобы встраивать гены, не вызывая болезни. Даже из ВИЧ можно сделать средство лечения болезней. Источник: U.S. National Library of Medicine
Лечение заболеваний сетчатки, как утверждается в сообщении издательства Mary Ann Liebert, Inc, оказывается той областью, где генная терапия проявит себя раньше- почему? Практическое подтверждение тому есть не только в недавно сделанной работе ученых на мышах, генная терапия авароза Лебера уже проверялась и на людях, но почему именно офтальмологами? А не, к примеру, онкологами или кардиологами, ведь от болезней сердечно-сосудистой системы и рака умирает больше всего пациентов во всем мире?
Ответ на этот вопрос таков: до сетчатки сравнительно несложно добраться, а ее форма и размеры облегчают попадание несущего нужный ген вируса в достаточное количество клеток. Кроме того, ученым известно, какие именно гены часто оказываются дефектными при том или ином поражении светочувствительных клеток, то есть им известно, какие гены необходимы внедрять в используемые при терапии вирусы.
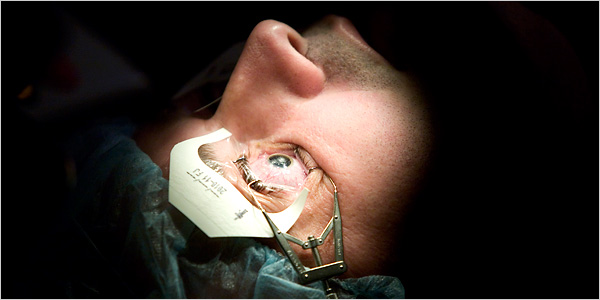
Хирургические операции на глазах традиционно считаются одними из наиболее сложных и тонких. Однако для генной терапии сетчатка - один из самых простых случаев, так как до нее проще добраться, чем, к примеру, до печени или головного мозга. Источник: innovation.freedomblogging.com
От чего лечили
Амавроз Лебера, от которого лечили подопытных мышей, является сравнительно редким заболеванием, от него страдает один новорожденный на 81 тысячу. Мутация в одном из 11 генов (среди которых и упомянутый выше RPGRIP1) приводит к тому, что в сетчатке нарушается развитие светочувствительных клеток- глаз уже в первые месяцы жизни утрачивает способность не только видеть, но и реагировать на свет.
Детальное изучение генетических основ болезни, проведенное ранее медиками (болезнь изучают с XIX века) позволило найти эти 11 генов, а развитие генной инженерии помогло и встроить ген RPGRIP1 в вирус, которым заразили клетки сетчатки. Слово «заразили», конечно, сложно ассоциировать с лечением, но необходимо подчеркнуть, что вирус был далеко не простой: его способность внедрять свои гены в ДНК клетки стала ключевой для всей терапии.
Важная деталь!
Особое внимание требуется обратить на то, что амавроз Лебера вызывается мутацией в одном из 11 генов. Иными словами, найденное учеными решение не универсально, а сработает лишь в части случаев- что, впрочем, не повод для разочарований. В прошлом году была опубликована другая работа, также посвященная этой болезни и генной терапии- но не за счет замены гена RPGRIP1, а за счет гена RPE65. Два гена из 11 за год, такими темпами можно рассчитывать на то, что лет через десять удастся перейти от первых опытов к стандартным операциям.
Никакими иными способами медики не смогли бы в достаточное число клеток (это миллионы, если не десятки и сотни миллионов!) доставить нужный ген и «вклеить» его в ДНК. Вирус же сделал это самостоятельно, а об отсутствии побочных эффектов позаботились ученые, лишившие его способности вызывать развитие болезни.
Другие варианты
Генная терапия- важный, но единственный метод, способный в будущем решить проблему слепоты. Наряду с ней ученые работают в других направлениях, создавая, например, протезы сетчатки. Электронная светочувствительная матрица, во многом схожая с матрицей цифрового фотоаппарата, преобразует свет в электрические импульсы, а специальная микросхема преобразует эти импульсы в сигналы, которые уже можно передать непосредственно на зрительный нерв. Если у пациента по каким-то причинам вышла из строя сетчатка, но ведущие к мозгу нервные волокна уцелели, этот способ может помочь увидеть если не полноценное изображение, то хотя бы картинку, позволяющую самостоятельно передвигаться по дому и улице.
Источник: gzt.ru